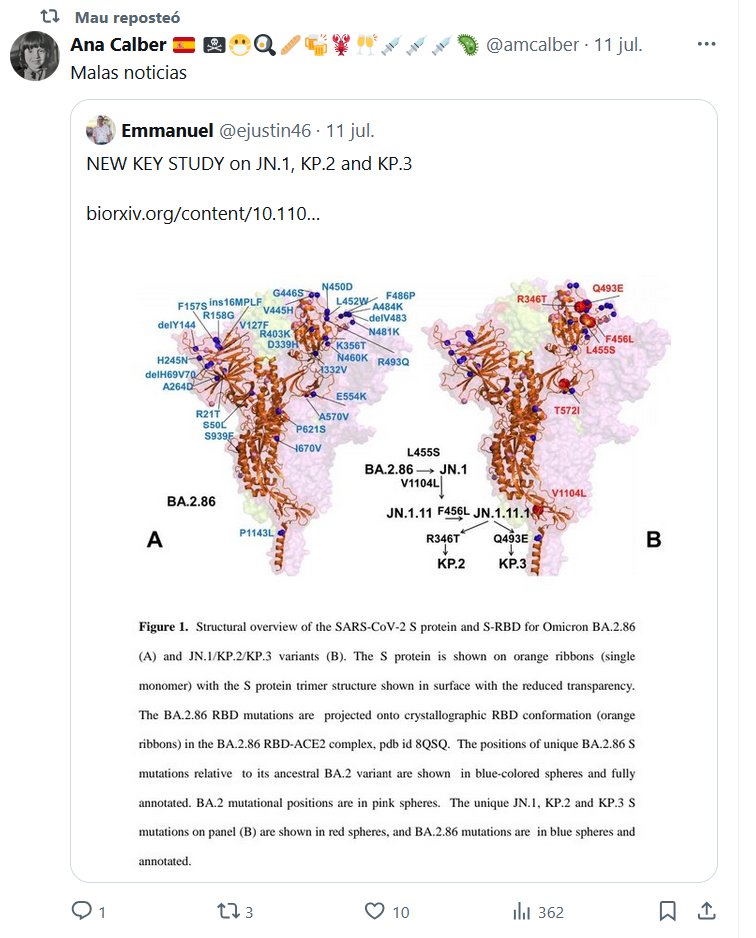
https://www.biorxiv.org/content/10.1101/2024.07.09.602810v1
Abstract
La ola más reciente de variantes Omicron del SARS-CoV-2 que descienden de BA.2 y BA.2.86 exhibió un crecimiento y una aptitud viral mejorados debido a la evolución convergente de los puntos críticos funcionales. Estos puntos críticos operan en conjunto para optimizar la unión del receptor para una infección efectiva y la eficiencia de la evasión inmune, manteniendo así la aptitud viral general. La falta de detalles moleculares sobre la estructura, la dinámica y la energía de unión de las últimas variantes FLiRT y FLuQE con el receptor ACE2 y los anticuerpos supone un desafío considerable que se explora en este estudio. Combinamos predicciones atomísticas basadas en AlphaFold2 de estructuras y conjuntos conformacionales de los complejos Spike del SARS-CoV-2 con el receptor huésped ACE2 para las variantes de Omicron más dominantes JN.1, KP.1, KP.2 y KP.3 para examinar la Mecanismos subyacentes al papel de los puntos críticos de evolución convergente en el equilibrio de la unión de ACE2 y la evasión de anticuerpos. Utilizando el escaneo mutacional basado en conjuntos de los residuos de proteínas de pico y los cálculos de las afinidades de unión, identificamos puntos críticos de energía de unión y caracterizamos las bases moleculares subyacentes a los acoplamientos epistáticos entre puntos críticos mutacionales convergentes. Los resultados sugirieron la existencia de interacciones epistáticas entre sitios mutacionales convergentes en las posiciones L455, F456, Q493 que permiten proteger y restaurar la afinidad de unión de ACE2 al tiempo que confieren un escape inmunológico beneficioso. Para examinar los mecanismos de escape inmunológico, realizamos un perfil mutacional basado en la estructura de la unión de la proteína de pico con varias clases de anticuerpos que mostraban una neutralización deteriorada contra BA.2.86, JN.1, KP.2 y KP.3. Los resultados confirmaron los datos experimentales de que JN.1, KP.2 y KP.3 que albergan las mutaciones L455S y F456L pueden perjudicar significativamente la actividad neutralizante de los anticuerpos monoclonales de clase 1, mientras que los efectos epistáticos mediados por F456L pueden facilitar la convergencia posterior de Q493E cambia para rescatar el enlace ACE2. El análisis estructural y energético proporcionó una justificación a los resultados experimentales que muestran que los anticuerpos BD55-5840 y BD55-5514 que se unen a diferentes epítopos de unión pueden conservar la eficacia neutralizante contra todas las variantes examinadas BA.2.86, JN.1, KP.2 y KP.3. . Los resultados respaldan la idea de que la evolución de las variantes de Omicron puede favorecer la aparición de linajes con combinaciones beneficiosas de mutaciones que involucran mediadores de acoplamientos epistáticos que controlan el equilibrio de la alta afinidad de ACE2 y la evasión inmune.